أنشئ حسابًا أو سجّل الدخول للانضمام إلى مجتمعك المهني.

Because of the difference in the ionic radius, since Ni (II) is a smaller metal ion with the electronic configuration [Ar]3d^8; it has only three main electronic levels (Which means higher density of the positive charge), that’s why it can adapt four Chloride ligands around it forming a tetrahedral structure.
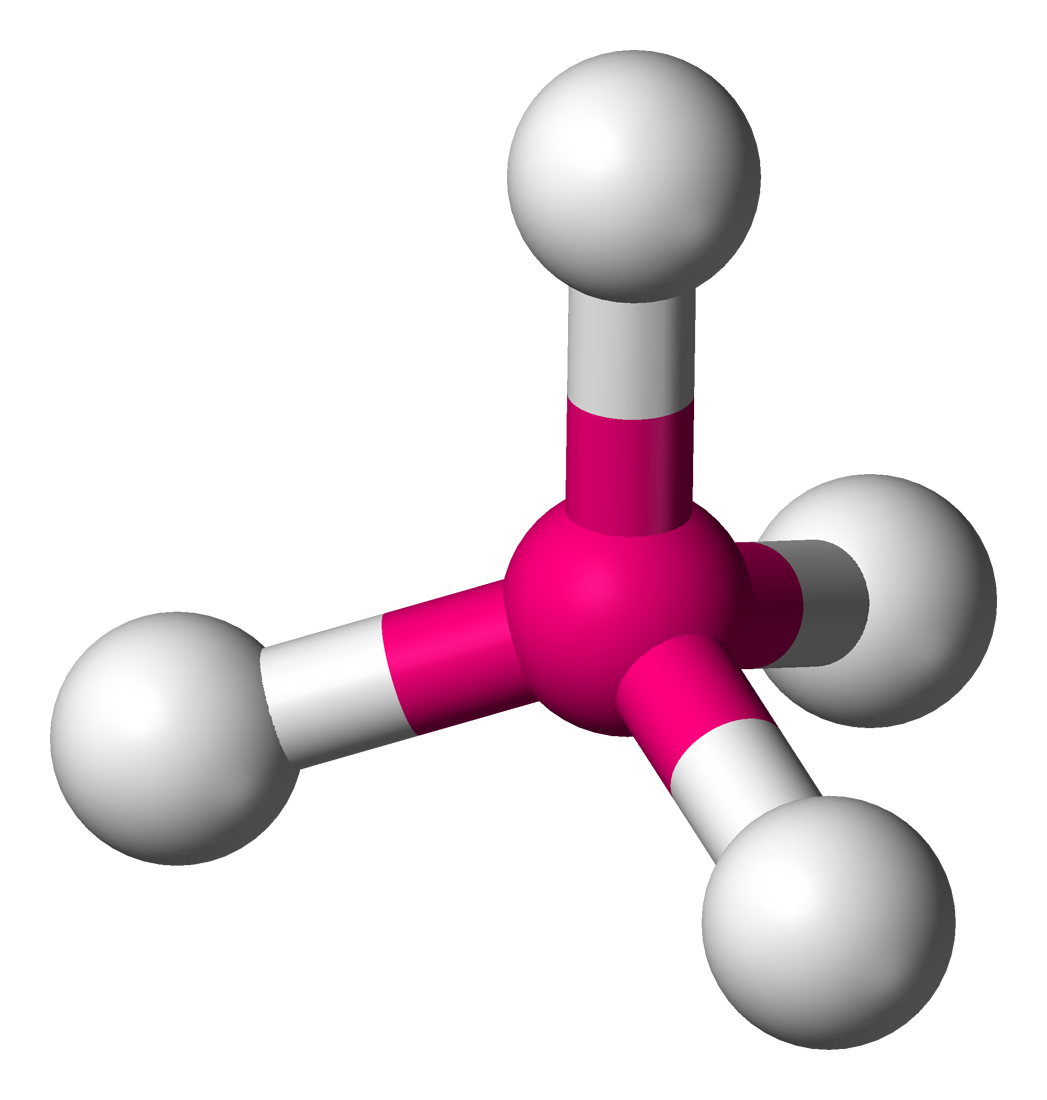
While Pt is a larger metal ion with the electronic configuration [Xe] 4f^14,5d^8; It has five electronic levels with a completely filled f orbitals (which blocks the positive charge of the nucleus), that’s why it’s too large to adapt the tetrahedral structure so it accommodates the four Chloride ligands as a square planar.






هل تحتاج لمساعدة في كتابة سيرة ذاتية تحتوي على الكلمات الدلالية التي يبحث عنها أصحاب العمل؟